 In den vergangenen Jahren hat sich in der Behandlung von Nierenkrebs sehr viel verändert. Mitte 2006 wurden die ersten Vertreter der sogenannten zielgerichteten Therapien (Target-Therapien) in Deutschland zugelassen. Dabei handelt es sich um Medikamente, die gezielt auf Tumorzellen wirken und so das Wachstum und eine weitere Streuung des Krebses verhindern. Sie werden meist als Tabletten oder Kapseln verabreicht.
In den vergangenen Jahren hat sich in der Behandlung von Nierenkrebs sehr viel verändert. Mitte 2006 wurden die ersten Vertreter der sogenannten zielgerichteten Therapien (Target-Therapien) in Deutschland zugelassen. Dabei handelt es sich um Medikamente, die gezielt auf Tumorzellen wirken und so das Wachstum und eine weitere Streuung des Krebses verhindern. Sie werden meist als Tabletten oder Kapseln verabreicht.
Im Gegensatz zur klassischen Chemotherapie sind diese Medikamente weniger schädlich für die „normalen, gesunden“ Zellen. Heute wissen wir, wie sich Krebszellen entwickeln und wie sie sich von gesunden Zellen unterscheiden. Dieses Wissen macht man sich bei den zielgerichteten Therapien zu nutze. Hat ein Tumor zum Beispiel eine bestimmte Größe erreicht, benötigt er Sauerstoff und Nährstoffe aus dem Blut, um weiter zu wachsen. Aus diesem Grund regen die Krebszellen das umliegende Gewebe dazu an, Blutgefäße zu bilden. Genau an dieser Stelle greifen einige der neuen Medikamente ein und verhindern gezielt die Neubildung der Blutgefäße. Der Tumor hungert quasi aus.
Andere Wirkstoffe stören die Signalübermittlung von Zellen und unterbinden so die Weiterleitung von Wachstumsfaktoren. Die Zellen können sich nicht mehr teilen und sterben teilweise sogar ab. Das Tumorwachstum wird dadurch gehemmt. Auf den folgenden Seiten möchten wir kurz auf die Wirkmechanismen der unterschiedlichen zielgerichteten Therapien für Nierenkrebs eingehen.
Weiter zu Tyrosinkinase-Inhibitoren (TKI)
Die neuste Art der Immuntherapie, die auch in der Behandlung des metastasierten Nierenzellkarzinoms eigesetzt wird, ist die Therapie mit speziellen Antikörpern, den sogenannten Immuncheckpoint-Hemmern. Um sie von der ursprünglichen Immuntherapie abzugrenzen, wird sie als immunonkologische Behandlung bezeichnet.
Wirkweise der immunonkologischen Behandlung
Unser Immunsystem verfügt über verschiedene Signalwege, über die eine Immunreaktion ausgelöst werden kann. Beispielsweise wird bei einer Virusinfektion das Immunsystem aktiviert, damit die krankheitsverursachenden Viren abgetötet werden. Jedoch gibt es auch Signalwege, die das Immunsystem hemmen. So können Autoimmunreaktionen, also ein Angreifen der körpereigenen Zellen, vermieden werden. Bei einer Erkältung wird beispielsweise das Immunsystem aktiviert, um die krankmachenden Keime zu vernichten. Wenn die Erkrankung vorbei ist, wird das Immunsystem heruntergebremst. Das Bremsen des Immunsystems ist wichtig, da sich sonst die Immunzellen gegen gesunde, körpereigene Zellen richten können und sogenannte Autoimmunreaktionen auslösen.
Das „Bremsen“ des Immunsystems geschieht über die sogenannten Immuncheckpoints (Kontrollstellen, vom englischen Begriff Checkpoint). Krebszellen besitzen die Fähigkeit diese Immuncheckpoints für sich auszunutzen. Sie senden Signale und aktivieren die Immuncheckpoints, wodurch die Immunzellen, die den Tumor erkennen und bekämpfen sollen, stark geschwächt werden. Ergebnis: Der Tumor trickst das eigene Immunsystem aus, so dass er unerkannt wachsen kann. Die sogenannten Immuncheckpoint-Hemmer wirken dem entgegen: Sie verhindern die Unterdrückung der Immunantwort durch den Tumor, so dass dieser vom Immunsystem erkannt und angegriffen wird.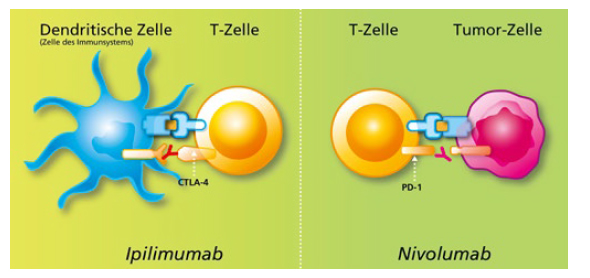
Die Forscher James Allison und Tasuku Honjo waren wesentlich an der Entwicklung von Checkpoint-Inhibitoren beteiligt. Für ihre Arbeit wurden sie im Jahr 2018 mit dem Nobelpreis für Medizin ausgezeichnet. Checkpoints, von denen man heute weiß, dass sie beim Nierenzellkarzinom eine Rolle spielen sind: PD-1, PDL-1 und CTLA-4. Seit April 2016 gibt es eine Zulassung für den Immuncheckpoint-Hemmer Nivolumab (Opdivo®) zur Behandlung des metastasierten (vorbehandelten) Nierenzellkarzinoms bei Erwachsenen in Zweitlinie. Das heißt, Patienten erhalten die Therapie mit Nivolumab, nachdem sie bereits eine Therapie mit einem Tyrosinkinase-Inhibitor erhalten haben. Im Januar 2019 wurde die Kombinationstherapie von zwei Immun-Checkpoint-Hemmern, Nivolumab (Opdivo®) und Ipilimumab (Yervoy®) zur Erstlinientherapie für metastasierte Nierenkrebs-Patienten der mittleren und ungünstigen Risikogruppe zugelassen.
Nebenwirkungen
Im Vergleich zu den zielgerichteten Therapien zeigen die neuen Immuntherapeutika im Allgemeinen weniger Nebenwirkungen. Allerdings können sie zu Beschwerden führen die durch Entzündungsmechanismen im Körper hervorgerufen werden und eine medikamentöse Behandlung dringend nötig machen. Dabei ist es nicht selten, dass sich eigentlich nur leichte Nebenwirkungen relativ schnell verschlimmern. Bereits bei geringen Beschwerden sollte deshalb zeitnah ein/e Arzt/Ärztin aufgesucht werden.
Folgende Nebenwirkungen sollten Sie umgehend mit Ihrem/Ihrer Arzt/Ärztin besprechen:
 Atmung: Kurzatmigkeit, erschwertes Ausatmen, Husten, rasselnde Atmung
Atmung: Kurzatmigkeit, erschwertes Ausatmen, Husten, rasselnde Atmung- Haut: Juckreiz, Ausschlag, Abschälen der Haut, Hautabschürfungen
- Magen-Darm-Trakt: Veränderungen der normalen Darm-Tätigkeit (Verstopfung, Durchfall), Blut oder Schleim im Stuhl, Bauchschmerzen, Schwindel, Erbrechen, Gewichtsverlust
- Augen: Entzündungserscheinungen im Augenbereich, Einschränkungen des Sehfeldes
- Neurologische Erscheinungen: sensorische Beschwerden (Kribbeln, Taubheitsgefühl in den Armen/Beinen), motorische Einschränkungen (Probleme beim Gehen, Gleichgewichtsstörungen)
- Allgemeinzustand: Fieber, Müdigkeit, starke Abgeschlagenheit, Kopfschmerzen, Austrocknung (Dehydrierung), Schockzustand, Verhaltensveränderungen, niedriger Blutdruck, Herzrhythmusstörungen
- Abnorme Laborwerte (werden vom Arzt festgestellt):
o Niere: Veränderungen des Kreatinin-Wertes
o Leber: erhöhte Blutwerte (AST, ALT, Bilirubin)
o Bauchspeicheldrüse: erhöhte Lipase-Werte
o Schilddrüse: veränderte TSH-Werte
o Störungen im Elektrolythaushalt
Wichtig: Nebenwirkungen können teilweise auch noch Monate nach Beendigung der Therapie auftreten.
Weiter zu Zielgerichtete Therapien
Das Nierenzellkarzinom gilt als sogenannter immunabhängiger Tumor. Daher war die Standardbehandlung beim metastasierten Nierenzellkarzinom bis zum Jahr 2006, als es noch keine zielgerichteten Therapien gab, die Immun- beziehungsweise Immunchemotherapie. Diese kombinierte die Zytokine (Botenstoffe des Immunsystems) Interferon-alpha (Roferon A®) und Interleukin-2 (Proleukin®) mit oder ohne Zugabe eines Chemotherapeutikums (5-FU).
Die Therapie führt zu einer allgemeinen (unspezifischen) Stimulation des Immunsystems mit dem Ziel der Zerstörung der Metastasen. Beide Botenstoffe des Immunsystems aktivieren dabei die körpereigenen Abwehrzellen (T-Zellen). Interferon-alpha (Roferon A®) verhindert die Zellteilung und damit das Tumorwachstum, Interleukin-2 (Proleukin®) dagegen fördert das Zellwachstum und die Ausbildung von Zellen, die Krankheitserreger sofort angreifen (sogenannte immunologische Effektorzellen). Beide Wirkmechanismen scheinen sich zu ergänzen.
Nach Behandlung mit dieser Art der Immuntherapie waren Patient:innen in Einzelfällen über mehrere Jahre krankheitsfrei. Leider hatte diese Therapie jedoch auch viele Nachteile:
- nur klarzellige Nierenzellkarzinome waren für die Behandlung geeignet,
- nur 5 bis 20 Prozent der Patient:innen sprachen überhaupt auf die Therapie an,
- die Therapie war mit sehr starken Nebenwirkungen verbunden.
Da es heute vielfältige andere Therapien für das metastasierte Nierenzellkarzinom gibt, wird diese Methode nur noch in Ausnahmefällen, bei ausgewählten Patient:innen und unter strenger medizinischer Überwachung durchgeführt.
Weiter zu Immunonkologie
Bevor die behandelnden Ärzt:innen mit Ihnen über unterschiedliche Behandlungsmöglichkeiten sprechen können, müssen die Ergebnisse der verschiedenen Untersuchungen vorliegen – dies kann durchaus mehrere Tage dauern. In der Regel werden Ihnen - auf jeden Fall aber Ihrem/Ihrer behandelnden Arzt/Ärztin, alle Untersuchungsergebnisse zur Verfügung gestellt. Sammeln Sie von Beginn an alle Berichte, Befunde, Laborwerte, etc. Dabei hilft Ihnen das Ordner-Register, das Sie bei uns bestellen können. Die gesammelten Befunde sind wichtig für den Gesamtüberblick und auch für eine Zweitmeinung, sollte diese irgendwann nötig sein.
Hat Ihr/Ihre Arzt/Ärztin alle Untersuchungsergebnisse erhalten, weiß er/sie genau, welche Tumorart vorliegt und wie weit sich der Krebs bereits im Körper ausgebreitet hat beziehungsweise wie aggressiv er möglicherweise wächst. Für die verschiedenen Nierenkrebs-Arten stehen mittlerweile mehrere Behandlungsmöglichkeiten zur Verfügung.
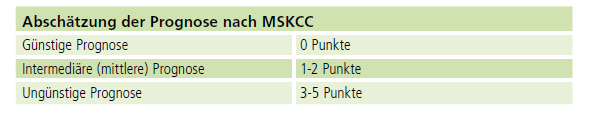
Grundlage für die Wahl der medikamentösen Therapie liefert letztendlich auch die sogenannte Prognoseabschätzung. Sie gibt an, wie hoch das Risiko ist, dass die Erkrankung fortschreitet. Für Nierenkrebs gibt es hierbei verschiedene Modelle. Sie erfassen unterschiedliche Faktoren, die im Zusammenhang mit dem Fortschreiten einer Erkrankung stehen. Das bekannteste Modell für den Einsatz der medikamentösen Therapien ist der sogenannte Motzer-Score (auch MSKCC genannt). Hierbei verwendet der/die behandelnde Arzt/Ärztin einfach festzustellende Laborwerte. Zur Abschätzung der Prognose wird dabei für jeden Risikofaktor ein Punkt vergeben und anschließend werden die Punkte zusammengezählt.
Die folgenden Werte werden betrachtet:
 Laktat-Dehydrogenase (LDH) über das 1,5fache des oberen Normwertes (1 Punkt)
Laktat-Dehydrogenase (LDH) über das 1,5fache des oberen Normwertes (1 Punkt)- Hämoglobin (HB) unter dem unteren geschlechtsspezifischen Normwert (1 Punkt)
- Blut-Kalzium-Spiegel: Korrigierter Wert über 10mg/dl (1 Punkt)
- Karnofsky Index unter 80 Prozent (Beurteilung des Allgemeinzustandes des Patienten) (1 Punkt)
- Der Primärtumor wurde nicht entfernt (1 Punkt)
- Weniger als ein Jahr nach der Erstdiagnose sind Metastasen aufgetreten (1 Punkt)
Werden nun alle Punkte zusammengezählt lässt sich die Prognose abschätzen:
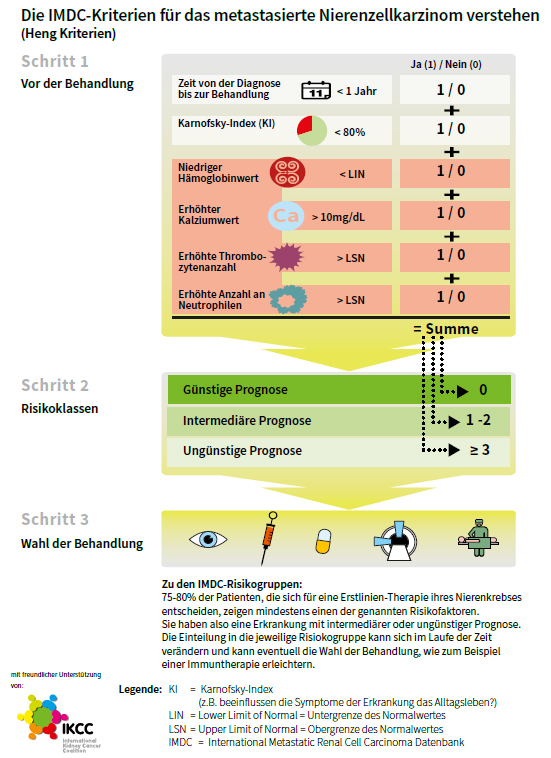
In den vergangenen Jahren wurde der Motzer-Score zunehmend von den IMDC-Kriterien nach Heng abgelöst. Hier wird das Risiko ähnlich berechnet wie bei Motzer. Je nachdem welcher Prognosegruppe Sie zugeordnet werden, stehen Ihnen unterschiedliche Behandlungsmöglichkeiten zur Verfügung.
Weiter zu Immunchemotherapie




 Herzlich Willkommen beim Nierenkrebs-Netzwerk Deutschland e.V.
Herzlich Willkommen beim Nierenkrebs-Netzwerk Deutschland e.V.







 © Nierenkrebs-Netzwerk Deutschland e.V. 2012-2023 |
© Nierenkrebs-Netzwerk Deutschland e.V. 2012-2023 | 